MTLAs, Ärzte und künstliche Intelligenz am MLL – ein gutes Team!
Zytomorphologie
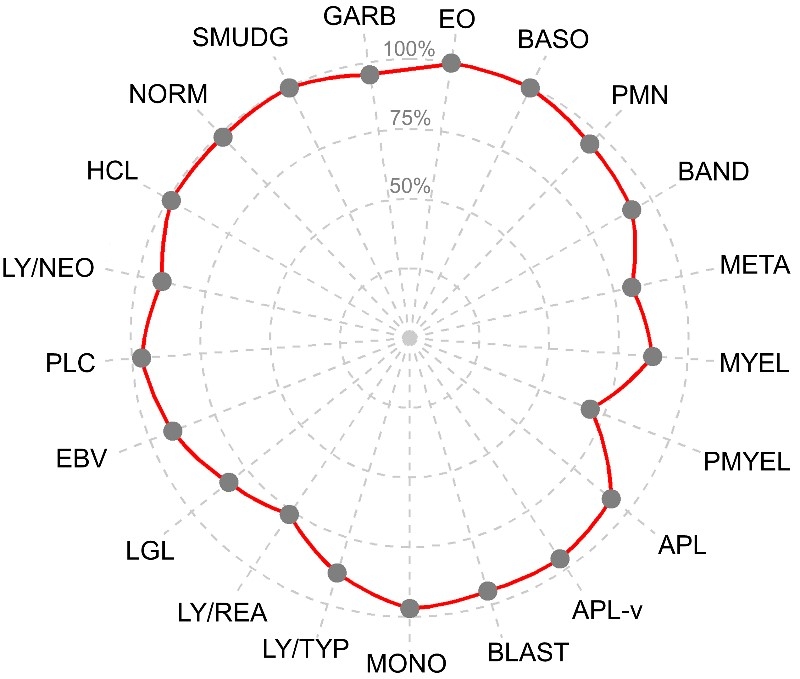
Immunphänotypisierung
Chromosomenanalyse

Molekulargenetik
Die Molekulargenetik spielt eine zunehmend wichtige Rolle in der Diagnostik. Insbesondere die Sequenzierung ermöglicht einen tiefen Einblick in die Biologie von Krankheitsbildern. Dabei stellen sich aber auch neue Herausforderungen. Nicht jede identifizierte Mutation ist von Relevanz für das Krankheitsbild. Bei der Einschätzung der Pathogenität kann der MLL Predictor, eine eigens entwickelte KI, den Diagnostiker wesentlich unterstützen.
Der nächste Schritt in der molekulargenetischen Diagnostik sind genomweite Ansätze. Jedoch übersteigen Daten, die durch Sequenzierung des kompletten Genoms und Transkriptoms entstehen, die Möglichkeiten manueller Auswertungen. Hier kann KI Abhilfe leisten und den Output dieser Daten deutlich erhöhen. Das MLL entwickelt in Kooperation mit AWS einen Algorithmus, der anhand von 5 Aberrationstypen eine Vorhersage zur Diagnose erstellt. Dafür werden genetische Strukturvarianten, Einzelnukleotid-Varianten (SNVs), Kopienzahlvarianten (CNVs), Genfusionen und Genexpressionsdaten in das Tool eingelesen und von der KI ausgewertet. Der Algorithmus hat bereits jetzt eine hohe Präzision, besonders bei genetisch eindeutigen Entitäten. Derzeitiges Training fokussiert sich zunehmend auf genetisch weniger klar definierte Entitäten, die den Algorithmus vor eine große Herausforderung stellen.
Die Autorin

»Sie haben Fragen zum Artikel oder wünschen weitere Informationen? Schreiben Sie mir gerne eine E-Mail.«
Dr. rer. nat. Constanze Kühn
Medical Writer